
(#42, #62)
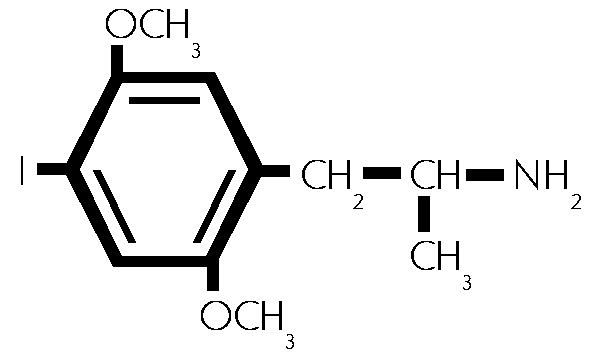
2,5-Dimethoxy -4- iodamphetamin, (#42/633, #62) 2,5- Dimethoxy -4- iod -phenyl-isopropylamin. (#62)
Die Summenformel lautet auf C11H16NO2I. Das Molekulargewicht betraegt 321,16. Die Droge ist ein farbloses Oel, das in Aether und HCl loeslich ist. Es bildet weisse Kristalle mit einem Schmelzpunkt (mp) von 200,5-201,5 Grad Celsius. (#62)
DOI ist von der chemischen Struktur her ein Amphetamin und unterscheidet sich damit nur durch eine Methylgruppe von dem Phenethylamin 2C-I. Beide haben den gleichen Substituenten an der 4. Position: ein Iodatom. Der gleiche Zusammenhang besteht auch bei 2C-B und DOB. 2C-B ist ein Phenethylamin und DOB das korrespondierende Amphetamin. Das gleiche gilt nochmals fuer 2C-C und DOC, wo gegenueber 2C-B und DOB das Bromatom an der 4. Position gegen ein Chloratom getauscht worden ist. Die nachfolgende Tabelle gibt den Zusammenhang zwischen Substitution, Wirkdauer, Wirkstaerke der einzelnen halogenierten Phenethylamine und Amphetamine an. Es ist uebrigens noch folgender Zusammenhang zu bemerken: Das Phenethylamin ist immer schwaecher als das korrespondierende Amphetamin, wie man auch gut aus der Tabelle ersehen kann: (eigen)
| Phenethylamin: | Amphetamin: | 4. Position: | ||||
| Name: | Dosis [mg]: | Dauer [h]: | Name: | Dosis [mg]: | Dauer [h]: | |
| 2C-B | 12-24 | 4-8 | DOB | 1-3 | 18-30 | Brom |
| 2C-C | 20-40 | 4-8 | DOC | 1,5-3 | 12-24 | Chlor |
| 2C-I | 14-22 | 6-10 | DOI | 1,5-3 | 16-30 | Iod |
Tabelle. Gegenueberstellung der bekannten halluzinogenen Phenethylamine und Amphetamine mit einem Halogenatom an der 4.Position des aromatischen Benzolringes. (Daten nach Alexander Shulgin: "PIHKAL.").
Wieder, wie mit jedem anderen halluzinogenen Amphetaminanalog, das ein chirales Zentrum hat, und in der individuellen optischen Isomerenform untersucht wurde, ist es das 'R' Isomer, dass potenter ist. Und wieder zeigt das andere Isomer, das 'S' Isomer, immer noch einige Aktivitaet. Das gleiche war wahr mit DOB, und DOM, und MDA. Die einzige Ausnahme war MDMA, aber dies ist auch mehr ein Stimulanz, und es gibt praktisch keine halluzinogene Komponente in seiner Wirkung. Studien mit Ratten, wo es gibt ein Mass der Unterscheidung von einem Teststoff von einer Salzloesung, haben gezeigt, dass das 'R' Isomer rund die zweifache Potenz des 'S' Isomers besitzt. Dass das 'R' potenter ist, ist sicher, aber die obigen Berichte wuerden nahelegen, dass der Faktor naeher am Vierfachen als am zweifachen liegt. Eine Zahl an Studien mit DOI in Tierversuchen haben gezeigt, dass es eine extrem hohe Bindungskapazitaet besitzt, zu dem, was der 5-HT2 Receptor genannt wird. Serotonin ist ein wesentlicher Neurotransmitter im Gehirn, und ist sehr stark in die Wirkung der Phenethylaminhalluzinogene verwickelt. Der Platz wo es wirkt, auf der molekularen Ebene, wird sein Rezeptorsitz genannt. Als ein Ergebnis der gemeinsamen Studien von medizinischen Chemikern, die sehr nahe zusammenarbeiteten mit Neuropharmakologen, ist eine Zahl von Verbingungen aufgetaucht, die mit diesem Plaetzen interagieren. Aber dieser eine interagiert mit diesen Platz und nicht mit diesem, und jener interagiert mit jenem Platz und nicht mit diesem. So, es hat sich eine Sammlung von Unterabteilungen und Unter-Unterabteilunge von Receptorsitzen entwickelt, alle verbunden mit Serotonin, aber jede definiert durch eine besondere Substanz, die am engsten mit diesem interagiert.
Folglich, gab es den Serotonin '1' Receptor, und dann gab es den '1' und '2' Receptor, und dann '1a' und '1b' und '2a' und '2b' Receptoren, und so fort. Diese werden 5-HT Receptoren genannt, da der chemische Name fuer Serotonin 5-Hydroxytryptamin ist. DOI wurde synthetisiert mit verschiedenen radioaktiven Iodisotopen, und diese Werkzeuge ware von beachtlichen Wert im Kartographieren der Gehirnverteilung. Und durch Extrapolation, wurde die moegliche Lokalisierung von anderen halluzinogenen Stoffen, die nicht so leicht markiert werden koennen, moeglich. Eine kleine neurochemische Forschungsfirma an der Ostkueste nahm diese Moeglichkeiten von DOI auf, und bot es als kommerziell erhaeltliches Produkt fuer die Forschung an. Aber ich zweifele, dass sie komplett unwissend der Tatsache sind, dass DOI ein sehr starkes, potentes Halluzinogen ist, und dass es immer noch nicht im Bundesdrogengestz erfasst ist, inzwischen, in ihrem neuesten Katalog, hat sich der Preis verdoppelt und eine Bemerkung wurde hinzugefuegt, dass Telefonbestellungen fuer diese Substanz nicht akzeptiert werden koennen.
Fuer jene, die solche Statistiken interessant finden, die Elternkomponente DOI gilt mit DOB als wahrscheinlich potenteste im Moment von allen Phenethylaminhalluzinogenen, und ist sicherlich eines der am laengsten wirkenden Phenethylamine. (#42/634ff.)
A. Shulgin hat folgende subjektiven Wirkberichte in seinem Werk "PIHKAL" gesammelt und veroeffentlicht:
0.6mg: Es gab eine feine vertraeumte, leichte Benommenheit fuer einige Stunden, und es schien, dass die Zeit langsam verging. Dann kam eine allgemeine Traurigkeit ueber mich, als ich mich an fruehere Tage erinnerte (Freuden zurueckrufend, die nun vergangen sind) und mich wunderte, ob es mir noch erlaubt sein wuerde hier auf der Farm zu sein, wenn ich alt und unwichtig bin. Es ist so viel zu tun, und ich kann es nicht alles tun, und niemand anderen kuemmert es. Meine Stimmmung wurde wieder gegenwaertig und gesund nach der siebenten Stunde.
3mg: Dies ist ein klares, sauberes Halluzinogen. Die Bilder, die man mit geschlossenen Augen sieht, sind ausgezeichnet, mit klar gezeichneten Mustern, Bildern und Farben. Perfekt fuer einen Kuenstler, und das naechste mal werde ich etwas Zeit zum Malen opfern. Totale Behaglichkeit fuer den Koerper, aber keine Hilfe fuer mein Rauchproblem. Ich wollte immer noch rauchen. Nach 16h auf DOI bin ich immer noch auf einem 1.5+, aber ich werde irgendwie versuchen zu Bett zu gehen, und zu schlafen.
3.5mg: Ich war auf einem vollen, fuerchterlichen +++ fuer rund 3-4h. Es gab keine von dem LSD-Funkeln, aber es gab Momente von 'leichter Benommenheit', wo man sich seitwaerts zur Realitaet bewegen konnte. Ich konnte den Ort verlassen, wo ich gerade dort war, und herueberkommen und eine eigenartige aber authentischen Sicht bekommen, wo das 'dort' war, dass ich verlassen hatte. Es wuerde ausserhalb des Koerpfer sein, ausgenommen, der Koerper kam herueber mit mir, eher als er dort bleiben wuerde. Dies macht nun keinen Sinn mehr, aber es machte ihn sicher. Es gab keine Spur von Koerperauswirkungen, und ich schlief spaet an diesen Abend, aber mit einiger Zurueckhaltung aufgrund der intensiven geistigen Bilder. Es war nicht intensiver als 3 mg, aber es war ein klein wenig mehr von der unrealen Seite.
1mg 'R' Isomer: Es war ein klares ++ von der zweiten bis zur achten Stunde, aber irgendwie war es nicht von der Eleganz oder dem Schub des Razemats. Ich war empfindlich, und managte den Haushalt zu machen mit einem vernuenftigen Weg. Einfacher Schlaf nach 15h Drogenwirkung.
2.3mg 'R' Isomer: Die Wasserloesung des Hydrochloridsalzes hatte einen leicht suesslichen Geschmack! Ich war auf einem +++ ohne Frage, aber es gab eine leicht niedergeschlagene Stimmung dem Ende zu. Und es dauerte eine wirklich lange Zeit; Ich war klar beeinflusst von dem restlichen Stoff, der noch in den naechsten Tag hinein wirkte.
6.3mg 'S' Isomer: Ich war auf einem gutartigen eineinhalb + nach rund 2h, und schliesslich ebnete aus auf einem ++. Wuerde ich diese Dosis verdoppeln? Wahrscheinlich nicht, aber die Haelfte nocheinmal (9-10mg) wuerde ein sicheres +++ sein. Am abend war ich nahe genug der Basislinie um in die Stadt zu fahren wegen einer sozialen Verpflichtung, aber sogar, wenn ich versuchte zu schlafen spaeter in dieser Nacht, gab es noch einige Reste geistiger Bilder; Bemerkenswert, alles war in langsamer Bewegung. Die Phantasien waren langsamschreitend und traege. Es waere interessant gewesen, das Augenschliessen waehrend des Tages zu untersuchen. (#42/634f.)
Der halluzinogene Wirkbereich wird von A. Shulgin mit 1,5-3mg der Rauschdroge angegeben. (#42/634, 62)
Die Dauer der Wirkung betraegt nach A. Shulgin 16-30h. (#42/634)
Die Ausbildung einer koerperlichen oder psychischen Abhaengigkeit ist nicht bekannt geworden. (eigen)
A. Shulgin gibt in seinem Wek "PIHKAL" folgende Synthese an:
Eine Mischung aus 14.8g Phthalanhydrid und 19.5g 2,5-Dimethoxyamphetamin als freie Base wurde nach und nach auf rund 150 Grad Celsius mit einer offenen Flamme erhitzt. Eine einzige klare Phase wurde durch den Verlust an H2O gebildet. Nachdem die heisse Schmelze fuer einige Momente ruhig geblieben war, liess man sie auf rund 50 Grad Celsius abkuehlen. Dann verduennte man mit 100ml heissem MeOH. Die Loesung wurde geruehrt, bis sie homogen war, mit einem Produktteil geimpft, und dann auf einem Eisbad gekuehlt, um die Kristallisation abzuschliessen. Nach dem Entfernen des Produkts durch Filtration, sparsamen Waschen mit MeOH und Lufttrocknen, wurden 24.6g N- (1- (2,5-Dimethoxyphenyl) -2- propyl) phthalimid, als gebrochen-weisse Kristalle, mit einem mp von 105-106 Grad Celsius erhalten.
Zu einer Loesung von 2g N- (1- (2,5-Dimethoxyphenyl) -2- propyl) phthalimid in 15ml warmer Essigsaeure, die kraeftig geruehrt wurde, wurde eine Loesung von 1.2g Iodmonochlorid in 3ml Essigsaeure hinzugefuegt. Dies wurde 2h lang bei rund 40 Grad Celsius geruehrt. Waehrend dieser Zeit gab es ein eindeutiges Hellerwerden der Farbe, aber keine Feststoffe entstanden. Die Reaktionsmischung wurde in 600ml H2O gegossen, dadurch entstand ein roetlicher Fleck, der in einer gelb-orangen, undurchsichtigen, waessrigen Phase herumfloss. Der Flecken wurde physikalisch entfernt, in 30ml kochendem MeOH geloest, beim Kuehlen auf einem Eisbad lagerten sich gebrochen-weisse Kristalle ab. Diese wurden durch Filtration entfernt, mit MeOH gewaschen, und Luftgetrocknet, um 1.5g N- [1- ( 2,5- dimethoxy -4- iodphenyl) -2- propyl] phthalimid als feine weisse Kristalle mit einer leicht purpurnen Schattierung zu erhalten. Der mp war 103-105.5 Grad Celsius und der gemischte mp mit dem am Beginn zugesetzten, nicht-iodierten Phthalimid (mp 105-106 Grad Celsius) war erniedrigt (85-98 Grad Celsius). Die Extraktion der waessrigen Phase, nach der Alkalisierung, ergab zusaetzliche 0.15g Produkt. Anal. (C19H18NO4) C,H,N.
Eine Loesung von 0.75g N- (1- (2,5-Dimethoxy -4- iodphenyl) -2- propyl) phthalimid in 10ml EtOH wurde mit 0.3 ml Hydrazinhydrat versetzt. Die klare Loesung wurde am Dampfbad eine Nacht lang am Rueckfluss gekocht. Nach dem Abkuehlen gab es eine Kristallisation von 1,4-Dihydroxyphthalizin, dass mit kleinen Perlen begann, aber schlussendlich sehr betraechtlich wurde und gerann. Diese Feststoffe wurden durch Filtration entfernt und hatten einen mp von rund 340 Grad Celsius (Das Belegbeispiel schmolz in einem im Bereich von 335-350 Grad Celsius). Das Filtrat wurde in 100ml CH2Cl2 geloest und mit 2x150ml 0.1N HCl extrahiert. Die waessrigen Extrakte wurden einmal mit CH2Cl2 gewaschen, mit 5%-iger NaOH basisch gemacht, und mit 3x100ml CH2Cl2 extrahiert. Das Entfernen des Loesungsmittels im Vakuum ergab 0.5g farbloses Oel, dass in 300ml wasserfreiem Et2O geloest und mit wasserfreiem HCl Gas gesaettigt wurde. Es wurden, nach Filtration und Lufttrocknen, 0.35g DOI-HCl als weisse Kristalle erhalten, die bei 200.5-201.5 Grad Celsius schmelzen. Dieser Wert verbesserte sich nicht durch Umkristallisieren. Anal. (C11H17ClINO2) C,H,N. (#42/633f.)
1991: Das Halluzinogen wird erstmalig durch A. Shulgin synthetisch hergestellt. (#62)